Leukozyten regulieren die Entwicklung von Lymphgefäßen
Forschungsbericht (importiert) 2010 - Max-Planck-Institut für molekulare Biomedizin
Das Verkehrsnetz unseres Körpers: die Blut- und Lymphgefäße
Das Blutgefäßsystem ist ein stark verzweigtes Netzwerk aus Arterien, Kapillaren und Venen, das sämtliche Gewebe des Körpers mit Sauerstoff und Nährstoffen, aber auch mit Hormonen, Botenstoffen, Wachstumsfaktoren und Zellen versorgt. Das Blutgefäßsystem ist daher für unsere Gesundheit von zentraler Bedeutung. Da der Blutkreislauf stets auf Hochdruck läuft, sind die Blutgefäße darauf spezialisiert, dem arteriellen Blutdruck zu widerstehen. Blutgefäße sind durch einen speziellen Zelltyp, Endothelzellen, ausgekleidet, der sehr dichte Zell-Zell-Verbindungen ausbildet. Darüber hinaus werden Blutgefäße durch Stützzellen und ein Geflecht aus Bindgewebsfasern stabilisiert. Trotzdem bewirkt der Blutdruck auf der arteriellen Seite des Gefäßsystems eine kontinuierliche Filtration von Flüssigkeit aus dem Blutplasma ins Gewebe. Der größte Anteil dieser Gewebsflüssigkeit wird auf der venösen Seite der Kapillaren reabsorbiert, die verbleibende Bindegewebsflüssigkeit wird zusammen mit im Gewebe befindlichen weißen Blutkörperchen von lymphatischen Gefäßen aufgenommen [1]. Im Gegensatz zu den Blutgefäßen ist das lymphatische Gefäßsystem kein geschlossener Kreislauf, sondern beginnt mit stumpf endenden, lymphatischen Kapillaren, welche sich zu zunehmend größeren Sammelgefäßen vereinigen. Der Ductus Thoracicus und der rechte Lymphgang schließen die jeweils größten lymphatischen Sammelgefäße an den venösen Ast des Kreislaufsystems an und sind die einzigen physiologischen Verbindungen zwischen beiden Gefäßsystemen.
Lymphatische Endothelzellen sind durch Filamente im Bindegewebe so verankert, dass bei Flüssigkeitseinlagerung ins Gewebe die sonst flachen Lymphgefäße röhrenförmig geöffnet werden und die Flüssigkeit in die lymphatischen Kapillaren eintritt. Entsprechend ihrer Funktion besitzen die Endothelzellen der lymphatischen Kapillaren keine dichten Zell-Zell-Verbindungen, sondern weisen spezielle, durchlässige Kontakte auf, die die Aufnahme von Gewebsflüssigkeit und weißen Blutkörperchen erleichtern. Die aus Interstitialflüssigkeit und weißen Blutkörperchen bestehende Lymphe passiert auf ihrem Weg in den venösen Kreislauf die Lymphknoten, in denen die weißen Blutkörperchen (angeborene Immunität) den Lymphozyten (adaptive Immunität) eventuell vorhandene Antigene präsentieren und damit Information über bestehende Infektionen weitergeben. Der Fluss der Lymphe erfolgt stets vom Gewebe über zunehmend großvolumigere Sammelgefäße in die venöse Zirkulation, wobei ein Rückfluss durch Klappen in den Sammelgefäßen unterbunden wird.
Blut- und Lymphgefäßsystem sind streng voneinander getrennt
Während der Embryonalentwicklung differenzieren die Endothelzellen des Lymphgefäßsystems aus dem venösen Endothel der Kardinalvene. Nachdem die Lymphendothelzellen von der Kardinalvene weggewandert sind, verläuft die Entwicklung beider Gefäßsysteme getrennt [2]. Diese strenge Trennung von Blut- und Lymphgefäßen ist aus zwei Gründen unverzichtbar. Zum einen kann nur so gewährleistet werden, dass Antigene, die Aufschluss über im Gewebe vorliegende Infektionen liefern, tatsächlich durch die Lymphknoten geleitet und dort von Lymphozyten erkannt werden. Lymphgefäße tragen daher entscheidend zur Funktion des Immunsystems bei. Zum anderen hat eine Reihe von gezielt erzeugten Mausmutanten gezeigt, dass Kurzschlüsse zwischen Blut- und Lymphkapillaren zu Ödemen, Blutungen und der Bildung von Ascites (Bauchwassersucht) führen, was sowohl während der Embryonalentwicklung als auch im Erwachsenenalter tödliche Komplikationen nach sich zieht. Dies ist leicht verständlich, wenn man bedenkt, dass Lymphgefäße aufgrund ihrer Architektur keine Druckstabilität aufweisen und dem arteriellen Blutdruck nicht widerstehen können [1].
Der Verlust verschiedener Gene führt in der Maus zu Kurzschlüssen zwischen Blut- und Lymphgefäßen
Für die Trennung der beiden Gefäßsysteme sind – wie die Mausmutanten zeigten – also bestimmte Gene verantwortlich. Erstaunlich war allerdings die Natur der Gene, deren Verlust zu Kurzschlüssen zwischen Blut- und Lymphgefäßen führte. Es handelte sich unter anderem um Proteine, die Signale in Leukozyten übermitteln, wie die zytoplasmatische Tyrosinkinase Syk, das Adaptorprotein SLP-76 und die Phospholipase PLC-γ sowie den Transmembranrezeptor CLEC-2. In neuer Zeit konnte auch gezeigt werden, dass der Verlust des Oberflächenproteins Podoplanin zu vergleichbaren Defekten führt. Podoplanin wird innerhalb des Gefäßsystems spezifisch von lymphatischen Endothelzellen ausgeprägt [3].
Defekte in Blutzellen führen zu vaskulären Pathologien
Um den Prozess der Trennung von Blut- und Lymphgefäßen besser zu verstehen, hat die Forschergruppe um Friedemann Kiefer die durch den Verlust der Kinase Syk verursachte Gefäßmissbildung im Detail untersucht. Dabei war zuerst die wesentliche Frage zu klären, ob die Kinase Syk während der Trennung von Blut- und Lymphgefäßen für die Funktion von Endothelzellen (man spricht von einer zellautonomen Funktion) oder die Funktion von Blutzellen (man spricht in diesem Fall von einer nicht-zellautonomen Funktion) wichtig ist. In der Fachliteratur war berichtet worden, dass aus dem Knochenmark abstammende Vorläuferzellen in Lymphendothelzellen differenzieren und sich dann in lymphatische Gefäße einlagern. Diese aus dem Knochenmark abstammenden Lymphendothelzellen seien nun bei Syk-Defizienz gestört. Durch genetisch veränderte Mäuse, in denen in allen Zellen, die normalerweise Syk ausprägen, nun ein farbiges Protein angeschaltet wird, konnte die Arbeitsgruppe der Max-Planck-Wissenschaftler jedoch eindeutig zeigen, (i) dass es keine Syk-exprimierenden Zellen im Knochenmark gibt, die lymphatisches Endothel bilden und (ii) dass der Defekt, der zu Kurzschlüssen von Blut- und Lymphgefäßen führt, ausschließlich auf Defekten in Blutzellen beruht (Abb. 1).
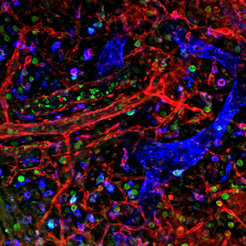
Weitere Untersuchungen zeigten dann, dass Blutzellen eine doppelte Funktion während der Bildung von Kurzschlüssen zwischen Blut- und Lymphgefäßen ausüben. So produzieren Syk-defiziente Makrophagen Wachstumsfaktoren, die das Lymphgefäßwachstum stark stimulieren, was unmittelbar die Bildung von Kurzschlüssen mit Blutgefäßen zu Folge hat. Zusätzlich sind Syk-defiziente Blutplättchen nicht in der Lage, solche Kurzschlüsse zu verschließen.
Makrophagen können Lymphgefäßwachstum stimulieren
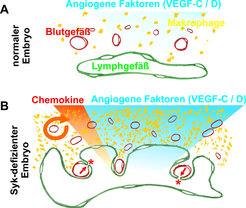
In Syk-defizienten Mausembryonen stellt man eine massive Anreicherung von Makrophagen in peripheren Geweben, z. B. in der Haut, fest [4]. Diese Makrophagen bilden sich aus Vorläuferzellen in der fötalen Leber und wandern über die Blutgefäße in die Peripherie ein. Am Zielort teilen sie sich nicht mehr. Es handelt sich um einen Makrophagen-Typ, der nicht mit Entzündungen assoziiert ist und als M2-polarisiert bezeichnet wird. Solche M2-Makrophagen befinden sich als Gewebe-residente Zellen in den meisten Geweben und erfüllen wichtige Funktionen in der Gewebeerhaltung (Homöostase). Sie eliminieren tote Zellen, unterstützen den Umbau von Geweben im Laufe von Alterungs- und Heilungsprozessen und können das Wachstum von Blut- und Lymphgefäßen stimulieren, indem sie sehr wirksame Wachstumsfaktoren ausschütten (Abb. 2 A).
Die Makrophagen, die in Syk-defizienten Embryonen akkumulieren, produzieren besonders hohe Mengen an – vor allem lymphangiogenen – Wachstumsfaktoren. Als Folge tritt eine massive Hyperplasie des Lymphendothels ein, das heißt dass Lymphendothelzellen sich wesentlich stärker teilen als zur Bildung von normalen Gefäßen nötig wäre. In der Folge entstehen massiv vergrößerte Lymphgefäße, die sackförmige Lagunen ausbilden und die Blutgefäße geradezu überwachsen. Dadurch kommen Blut- und Lymphendothelzellen in direkten physikalischen Kontakt (Abb. 2B). Im sich normal entwickelnden Embryo wird das Wachstum der beiden Gefäßtypen so gesteuert, dass dies nicht vorkommt. Interessanterweise bilden Blut- und Lymphgefäße, wenn sie in unmittelbarem physikalischen Kontakt stehen, Zell-Zellkontakte aus. Dies dürfte vor allem darauf zurückzuführen sein, dass beide Endothelzelltypen dieselben Moleküle für die Bildung ihrer Zell-Zell-Kontakte einsetzen. Die lymphangiogene Wirkung der M2-Makrophagen aus Syk-defizienten Embryonen konnte nachgewiesen werden, indem die Zellen aus der Haut eines Embryos in eine erwachsene Maus transplantiert wurden: dort stimulierten sie das Wachstum von Lymphgefäßen der Haut. Auch Makrophagen aus der Haut normaler Embryonen besitzen diese Fähigkeit, allerdings produzieren sie wesentlich weniger Wachstumsfaktoren, sodass viel mehr Zellen transferiert werden müssen, um eine Wirkung zu erzielen. Aus diesen Befunden kann man schließen, dass Makrophagen in der Lage sind, das Wachstum von Gefäßen – insbesondere von Lymphgefäßen – in der Embryonalentwicklung zu beeinflussen [4]. Im Erwachsenen war dies zuvor in verschiedenen Pathologien, wie z. B. Tumoren, bereits gezeigt worden.
Blutplättchen werden durch Lymphendothelzellen aktiviert
Unerwarteterweise konnten zeitgleich mehrere Arbeitsgruppen nachweisen, dass die Oberfläche von lymphatischen Gefäßen Blutplättchen aktiviert, also die Blutgerinnung auslöst. Dies kommt zustande, weil Blutplättchen einen Rezeptor für das selektiv auf der Oberfläche von Lymphendothelzellen ausgeprägte Protein Podoplanin besitzen. Podoplanin wird vom Rezeptor CLEC2 auf Blutplättchen erkannt und löst über diesen Rezeptor die Plättchenaktivierung aus. CLEC2 wiederum benötigt für seine Funktion die Kinase Syk [5].
Offensichtlich handelt es sich dabei um einen Sicherheitsmechanismus, der gewährleistet, dass Kurzschlüsse zwischen Blut- und Lymphgefäßen, wo immer sie entstehen, sofort wieder verschlossen werden. Neuere Ergebnisse legen nahe, dass solche Defekte im erwachsenen Leben immer wieder auftreten. Diese Kurzschlüsse müssen aktiv wieder verschlossen werden. Das übernehmen die Blutplättchen: nach deren Aktivierung bildet sich ein Thrombus, der die Öffnung zwischen den Gefäßsystemen abdichtet.
Gefäßpathologien sind potenzielle Nebenwirkungen bei Syk-Inhibition
Die Untersuchung der Gefäßdefekte in Syk-defizienten Mäusen, aber auch in anderen genetisch erzeugten Mutanten, hat unser Verständnis der Interaktion von Blut- und Lymphgefäßen wesentlich erweitert. Es ist klar geworden, dass die Trennung beider Gefäßsysteme, die während der Embryonalentwicklung angelegt wird, lebenslang aktiv aufrechterhalten werden muss. Insbesondere während entzündlicher Prozesse oder deren Ausheilung können Makrophagen zur Bildung neuer Kurzschlüsse führen. Eine gleichzeitige Einschränkung der Funktion von Blutplättchen, z. B. durch eine antikoagulante Therapie, kann somit fatale Folgen haben. Dies muss bei der Konzeption von Therapien, die auf veränderte Makrophagen oder Plättchenfunktionen abzielen, bedacht werden. So wird die Kinase Syk z. B. im Rahmen experimenteller Asthma- oder Allergietherapien inaktiviert; Veränderungen des Gefäßsystems bis hin zu lebensgefährlichen Blutungen könnten die Folge sein.

